Reconnection Equilibre Harmonie
Quand le corps retrouve son harmonie
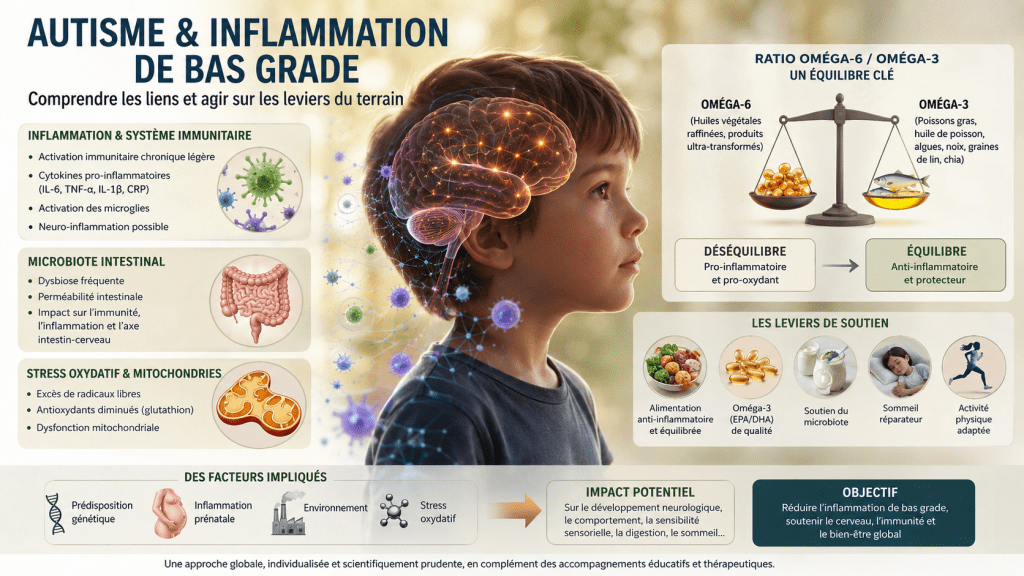
Autisme et inflammation chronique de bas grade

Autisme, inflammation chronique de bas grade et équilibre oméga‑6 / oméga‑3 : ce que montre réellement la recherche scientifique
Introduction
Depuis une quinzaine d’années, un nombre croissant de travaux scientifiques s’intéresse aux interactions entre le système immunitaire, l’inflammation chronique de bas grade, le microbiote intestinal et les troubles du neurodéveloppement. Parmi ces recherches, l’autisme — aujourd’hui désigné sous le terme de troubles du spectre de l’autisme (TSA) — occupe une place particulière.
Longtemps considéré uniquement sous l’angle génétique et neurologique, le TSA est désormais étudié dans une approche beaucoup plus globale intégrant :
- l’immunité,
- l’environnement,
- l’alimentation,
- le métabolisme,
- le microbiote,
- le stress oxydatif,
- la neuro‑inflammation,
- ainsi que l’équilibre des acides gras essentiels.
Parmi ces facteurs, le ratio oméga‑6 / oméga‑3 apparaît comme un sujet majeur.
Les chercheurs observent en effet qu’une alimentation occidentale moderne, très riche en oméga‑6 inflammatoires et pauvre en oméga‑3 marins, pourrait favoriser un terrain inflammatoire chronique susceptible d’influencer certaines fonctions cérébrales, immunitaires et comportementales.
Attention toutefois :
Les scientifiques ne considèrent pas l’autisme comme une simple maladie inflammatoire.
L’autisme reste un trouble neurodéveloppemental complexe, multifactoriel, fortement influencé par la génétique et le développement cérébral précoce.
Cependant, une partie des recherches suggère que l’inflammation chronique de bas grade pourrait participer à certains déséquilibres biologiques observés chez une partie des personnes TSA.
Comprendre l’inflammation chronique de bas grade
L’inflammation est un mécanisme normal de défense.
Lorsqu’une infection ou une agression survient, le système immunitaire active des cellules inflammatoires afin de protéger l’organisme.
Mais dans certaines situations, cette activation devient chronique, discrète et persistante. On parle alors d’inflammation chronique de bas grade.
Contrairement à une inflammation aiguë visible — comme une infection ou une blessure — cette inflammation silencieuse peut évoluer pendant des années sans symptôme évident.
Elle est aujourd’hui impliquée dans de nombreuses pathologies :
- diabète,
- maladies cardiovasculaires,
- obésité,
- dépression,
- maladies neurodégénératives,
- troubles auto‑immuns,
- et potentiellement certains troubles neurodéveloppementaux.
Les chercheurs utilisent différents biomarqueurs pour évaluer cet état inflammatoire :
- protéine C‑réactive ultrasensible (CRP‑us),
- interleukine‑6 (IL‑6),
- TNF‑alpha,
- IL‑1β,
- MCP‑1,
- cytokines pro‑inflammatoires.
Chez certaines personnes autistes, plusieurs études ont retrouvé une élévation légère mais chronique de certains de ces marqueurs.
Neuro‑inflammation et activation des microglies
L’un des mécanismes les plus étudiés concerne la neuro‑inflammation. Le cerveau possède ses propres cellules immunitaires : les microglies.
Ces cellules jouent un rôle fondamental dans :
- la protection neuronale,
- l’élimination des déchets cellulaires,
- la maturation cérébrale,
- la plasticité synaptique.
Mais lorsqu’elles restent activées de manière excessive, elles peuvent produire :
- cytokines inflammatoires,
- glutamate,
- radicaux libres,
- molécules oxydantes.
Certaines études post‑mortem réalisées chez des patients TSA ont montré une activation microgliale anormale dans plusieurs régions cérébrales.
Cette hyper‑activation pourrait théoriquement influencer :
- la communication neuronale,
- le traitement sensoriel,
- certaines fonctions sociales,
- l’équilibre excitation/inhibition du cerveau.
Les recherches restent prudentes, mais la neuro‑inflammation est aujourd’hui considérée comme un axe majeur d’investigation dans les TSA.
Stress oxydatif et dysfonction mitochondriale
Un autre élément fréquemment retrouvé dans la littérature scientifique concerne le stress oxydatif.
Le cerveau consomme énormément d’oxygène. Il est donc particulièrement vulnérable à l’excès de radicaux libres.
Plusieurs travaux ont retrouvé chez certains enfants TSA :
- une baisse du glutathion,
- une augmentation du stress oxydatif,
- des anomalies des enzymes antioxydantes,
- une dysfonction mitochondriale,
- une altération du métabolisme énergétique.
Or, inflammation chronique et stress oxydatif s’auto‑entretiennent. Plus l’inflammation augmente, plus les radicaux libres augmentent. Et plus les radicaux libres augmentent, plus l’inflammation est stimulée.
Ce cercle biologique pourrait contribuer à certains symptômes observés chez certains profils TSA.
Le microbiote intestinal : un axe central
Le lien intestin‑cerveau constitue aujourd’hui l’un des domaines les plus fascinants de la recherche.
Une proportion importante d’enfants autistes présente des troubles digestifs :
- constipation,
- douleurs abdominales,
- diarrhées,
- dysbiose,
- hypersensibilités alimentaires.
Le microbiote intestinal influence directement :
- le système immunitaire,
- la perméabilité intestinale,
- la production de neurotransmetteurs,
- l’inflammation,
- le métabolisme des acides gras,
- l’axe intestin‑cerveau.
Certaines bactéries intestinales produisent des métabolites capables d’agir directement sur le cerveau.
Des travaux expérimentaux suggèrent qu’une dysbiose pourrait favoriser :
- une activation immunitaire,
- une inflammation chronique,
- une augmentation de la perméabilité intestinale,
- une production accrue de molécules inflammatoires.
Ce domaine reste en pleine évolution, mais il constitue aujourd’hui une piste majeure dans la compréhension des interactions entre alimentation, inflammation et neurodéveloppement.
Pourquoi le ratio oméga‑6 / oméga‑3 est devenu un sujet majeur
- Les oméga‑3 et les oméga‑6 sont des acides gras polyinsaturés essentiels.
- Le corps humain ne peut pas les fabriquer correctement.
- Ils doivent donc être apportés par l’alimentation.
- Le problème ne vient pas des oméga‑6 eux‑mêmes.
Ces derniers sont indispensables au fonctionnement normal du cerveau, de l’immunité et des membranes cellulaires. Le problème vient surtout du déséquilibre moderne.
Dans les sociétés traditionnelles, le ratio oméga‑6 / oméga‑3 était probablement proche de :
- 1:1,
- 2:1,
- ou 4:1.
Aujourd’hui, dans de nombreux pays occidentaux, ce ratio dépasse fréquemment :
- 15:1,
- 20:1,
- parfois davantage.
Cette dérive provient principalement de :
- l’excès d’huiles végétales raffinées,
- des produits ultra‑transformés,
- de l’alimentation industrielle,
- de la baisse de consommation de poissons gras.
Comment les oméga‑6 peuvent influencer l’inflammation
Les oméga‑6, notamment l’acide arachidonique, servent à produire des molécules inflammatoires appelées eicosanoïdes.
Ces molécules jouent un rôle normal dans :
- l’immunité,
- la cicatrisation,
- la réponse aux infections.
Mais lorsqu’ils sont consommés en excès, certains oméga‑6 peuvent favoriser :
- une inflammation chronique,
- une activation immunitaire excessive,
- une production accrue de cytokines inflammatoires.
À l’inverse, les oméga‑3 marins EPA et DHA possèdent des propriétés généralement anti‑inflammatoires et neuroprotectrices.
Ils participent notamment à la production de :
- résolvines,
- protectines,
- médiateurs spécialisés de résolution de l’inflammation.
Autrement dit, les oméga‑3 ne bloquent pas l’inflammation normale. Ils aident plutôt l’organisme à revenir à l’équilibre.
Pourquoi les oméga‑3 intéressent les chercheurs dans les TSA
Le cerveau est extrêmement riche en DHA.
Cet oméga‑3 joue un rôle fondamental dans :
- la fluidité membranaire,
- les synapses,
- la transmission neuronale,
- le développement cérébral,
- la plasticité neuronale.
Plusieurs études ont retrouvé chez certains enfants TSA :
- des taux plus faibles d’oméga‑3,
- un déséquilibre lipidique,
- des anomalies des membranes cellulaires.
Les chercheurs se sont donc demandé si une amélioration du statut en oméga‑3 pouvait influencer certains symptômes. Forum témoignages Omega3 et Autisme
Certaines études rapportent des améliorations concernant :
- l’attention,
- l’irritabilité,
- l’hyperactivité,
- certaines fonctions sociales.
Les scientifiques pensent aujourd’hui que :
- certains profils biologiques pourraient répondre,
- tandis que d’autres non.
La variabilité génétique, immunitaire et métabolique semble probablement importante.
Le rôle possible de l’alimentation anti‑inflammatoire
De plus en plus de chercheurs explorent l’idée qu’un environnement métabolique moins inflammatoire pourrait soutenir certaines fonctions neurologiques.
Cela ne signifie pas « traiter » ou « guérir » l’autisme.
Mais plutôt optimiser le terrain biologique.
Parmi les approches étudiées :
- amélioration du ratio oméga‑6 / oméga‑3,
- réduction des aliments ultra‑transformés,
- alimentation riche en polyphénols,
- soutien du microbiote,
- amélioration du sommeil,
- activité physique adaptée,
- réduction du stress oxydatif.
Les chercheurs s’intéressent également à :
- la vitamine D,
- le magnésium,
- la choline,
- la phosphatidylsérine,
- certains antioxydants,
- les polyphénols alimentaires.
Prudence scientifique indispensable
Le sujet attire énormément d’attention sur internet. Mais il est essentiel de rester rigoureux.
À ce jour :
- aucune alimentation,
- aucun complément,
- aucun protocole anti‑inflammatoire,
- aucun oméga‑3
n’a démontré la capacité de « guérir » l’autisme mais cependant d’en atténué nombre de symptômes.
Les TSA sont des troubles neurodéveloppementaux complexes impliquant :
- génétique,
- épigénétique,
- environnement,
- développement cérébral précoce,
- immunité,
- métabolisme.
Les approches nutritionnelles doivent donc être considérées comme des pistes d’optimisation globale et non comme des traitements miracles.
Ce que montrent réellement les recherches
La littérature scientifique actuelle suggère plusieurs éléments cohérents :
- une partie des personnes TSA présente des signes biologiques d’inflammation légère,
- la neuro‑inflammation est activement étudiée,
- le microbiote pourrait jouer un rôle important,
- le stress oxydatif semble fréquent,
- les déséquilibres lipidiques et le ratio oméga‑6 / oméga‑3 intéressent fortement les chercheurs.
Cependant, les résultats restent hétérogènes.
Tous les patients TSA ne présentent pas ces anomalies.
Et les chercheurs ne disposent pas encore de preuves définitives permettant d’affirmer un lien causal unique.
Études et recherches scientifiques fréquemment citées
Neuro‑inflammation et microglies
- Vargas DL et al. (2005) — Neuroglial activation and neuroinflammation in the brain of patients with autism.
- Morgan JT et al. (2010) — Microglial activation and increased microglial density observed in autism.
- Suzuki K et al. (2013) — Microglial activation in young adults with autism spectrum disorder.
Cytokines inflammatoires
- Ashwood P et al. (2011) — Elevated cytokine levels in autism spectrum disorders.
- Goines P et al. (2011) — Increased inflammatory markers in children with autism.
- Masi A et al. (2015) — Cytokine abnormalities in autism spectrum disorder.
Stress oxydatif et mitochondries
- Chauhan A et Chauhan V (2006) — Oxidative stress in autism.
- Rossignol DA et Frye RE (2012) — Mitochondrial dysfunction in autism spectrum disorders.
- Frustaci A et al. (2012) — Oxidative stress‑related biomarkers in autism.
Microbiote intestinal
- Finegold SM et al. (2010) — Gastrointestinal microflora studies in late‑onset autism.
- Kang DW et al. (2013) — Reduced bacterial diversity in autism.
- Sharon G et al. (2019) — Human gut microbiota from autism spectrum disorder promote behavioral symptoms in mice.
Test du microbiote intestinal par un test sanguin et équilibrage du microbiote
Oméga‑3 et lipides membranaires
- Bell JG et al. (2004) — Fatty acid composition in autistic spectrum disorders.
- Patrick RP et Ames BN (2015) — Vitamin D and omega‑3 interactions in brain development and autism.
- Mazahery H et al. (2017) — Omega‑3 fatty acid supplementation in children with autism spectrum disorder.
Inflammation maternelle et neurodéveloppement
- Patterson PH (2011) — Maternal infection and immune involvement in autism.
- Brown AS et Patterson PH (2011) — Maternal infection and risk of autism.
- Estes ML et McAllister AK (2016) — Maternal immune activation and neurodevelopmental disorders.
Conclusion
Les liens entre autisme, inflammation chronique de bas grade et équilibre oméga‑6 / oméga‑3 constituent aujourd’hui un domaine scientifique extrêmement actif.
Les recherches suggèrent qu’une partie des personnes TSA pourrait présenter :
- une activation immunitaire légère,
- une neuro‑inflammation,
- un stress oxydatif,
- une dysbiose intestinale,
- des déséquilibres lipidiques.
Le ratio oméga‑6 / oméga‑3 apparaît comme un élément potentiellement important dans cette dynamique biologique.
Les oméga‑3 EPA et DHA intéressent particulièrement les chercheurs pour leurs propriétés anti‑inflammatoires, neuroprotectrices et membranaires.
Cependant, la science reste prudente. L’autisme ne peut pas être réduit à une simple inflammation chronique, malgré des pistes sérieuses liée à l’inflammation de bas grade.
Il s’agit d’un trouble neurodéveloppemental complexe dont les mécanismes impliquent simultanément génétique, immunité, métabolisme, soins liés à la parasitose, environnement et développement cérébral précoce.
Les approches nutritionnelles doivent donc être envisagées comme des outils potentiels d’optimisation globale du terrain biologique, et non comme des solutions miracles.
Même si aucune approche nutritionnelle ou anti-inflammatoire n’a démontré la capacité de « traiter » ou de « guérir » les troubles du spectre de l’autisme, un nombre croissant de chercheurs considère aujourd’hui que l’optimisation du terrain biologique pourrait représenter une piste complémentaire intéressante chez certains profils.
Dans cette logique, plusieurs axes sont régulièrement étudiés : amélioration du ratio oméga-6 / oméga-3, soutien du microbiote intestinal, réduction des aliments ultra-transformés, amélioration du sommeil, diminution du stress oxydatif et correction d’éventuelles carences nutritionnelles.
Les oméga-3 EPA et DHA intéressent particulièrement la recherche en raison de leur rôle majeur dans la fluidité des membranes neuronales, la communication synaptique et la résolution physiologique de l’inflammation.
Certains travaux suggèrent qu’un environnement métabolique moins inflammatoire pourrait contribuer à soutenir certaines fonctions neurologiques, immunitaires et digestives chez une partie des personnes TSA.\n\nCependant, la prudence scientifique reste indispensable.
L’autisme demeure un trouble neurodéveloppemental complexe impliquant simultanément génétique, développement cérébral précoce, immunité, environnement et métabolisme.
Le déparasitage a libéré de nombreux cas des symptômes les plus invalidant pour les patients qui sans le savoir étaient infestés cérébralement, l’incidence est dans ce cas facile à comprendre et parfois effrayante.
Les approches nutritionnelles ou métaboliques doivent donc être envisagées comme des stratégies globales de soutien du terrain physiologique, et non comme des solutions miracles.
Les chercheurs insistent également sur l’importance d’éviter les protocoles extrêmes, les régimes très restrictifs prolongés ou les promesses de guérison sans fondement scientifique.
L’objectif le plus raisonnable aujourd’hui consiste plutôt à favoriser un meilleur équilibre inflammatoire, digestif et métabolique susceptible d’améliorer le confort physiologique général et la qualité de vie de certaines personnes concernées.