Reconnection Equilibre Harmonie
Quand le corps retrouve son harmonie
Neuropathie et inflammation chronique de bas grade
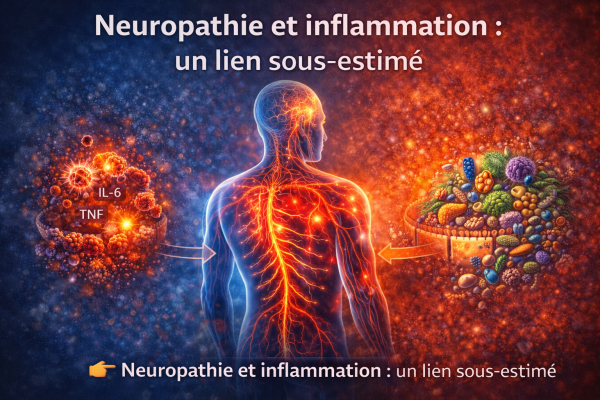
Neuropathie et inflammation chronique de bas grade : mécanismes physiopathologiques et stratégies intégratives
Résumé
La neuropathie, caractérisée par une atteinte des nerfs périphériques ou centraux, est de plus en plus associée à un état d’inflammation chronique de bas grade.
Les données récentes suggèrent que des facteurs tels que la dysbiose intestinale, la perméabilité intestinale et l’activation immunitaire persistante contribuent à la sensibilisation nerveuse et à la chronicisation de la douleur.
Cette revue examine les mécanismes impliqués et propose une approche intégrative combinant interventions nutritionnelles, modulation du microbiote et soutien neuro-métabolique.
1. Introduction
La neuropathie regroupe un ensemble de troubles affectant les nerfs, se manifestant par :
- douleurs
- brûlures
- picotements
- perte de sensibilité
Traditionnellement associée au diabète ou à des causes toxiques, elle est aujourd’hui replacée dans un contexte plus large : celui du terrain inflammatoire chronique.
Comme le souligne David Furman :
« L’inflammation chronique de bas grade est un facteur majeur de nombreuses maladies chroniques. »
Une nouvelle compréhension de la neuropathie
La neuropathie périphérique est traditionnellement décrite comme une atteinte structurelle des nerfs liée à des causes métaboliques, toxiques ou carentielles. Cependant, les données récentes indiquent qu’un état d’inflammation chronique de bas grade joue un rôle central dans son développement et sa progression.
Cette inflammation systémique persistante est caractérisée par une élévation modérée mais continue de cytokines pro-inflammatoires, contribuant à une altération de la fonction neuronale et à une sensibilisation nociceptive.
👉 Ainsi, la neuropathie doit être envisagée non seulement comme une pathologie nerveuse, mais comme l’expression d’un déséquilibre systémique du terrain biologique.
Références :
Furman D et al. Nat Med. 2019.
Ziegler D. Lancet Neurol. 2008.
2. Physiopathologie de la neuropathie
2.1 Atteinte nerveuse périphérique
La neuropathie périphérique implique :
- dégénérescence axonale
- atteinte de la myéline
- altération de la conduction nerveuse
2.2 Sensibilisation neuronale
Les nerfs deviennent hyperréactifs :
- seuil de douleur abaissé
- activation spontanée
- amplification du signal
3. Rôle central de l’inflammation chronique
3.1 Cytokines pro-inflammatoires
Les principales molécules impliquées :
- IL-6
- TNF-α
- IL-1β
👉 Effets :
- altération des fibres nerveuses
- activation des récepteurs de la douleur
- maintien de la neuropathie
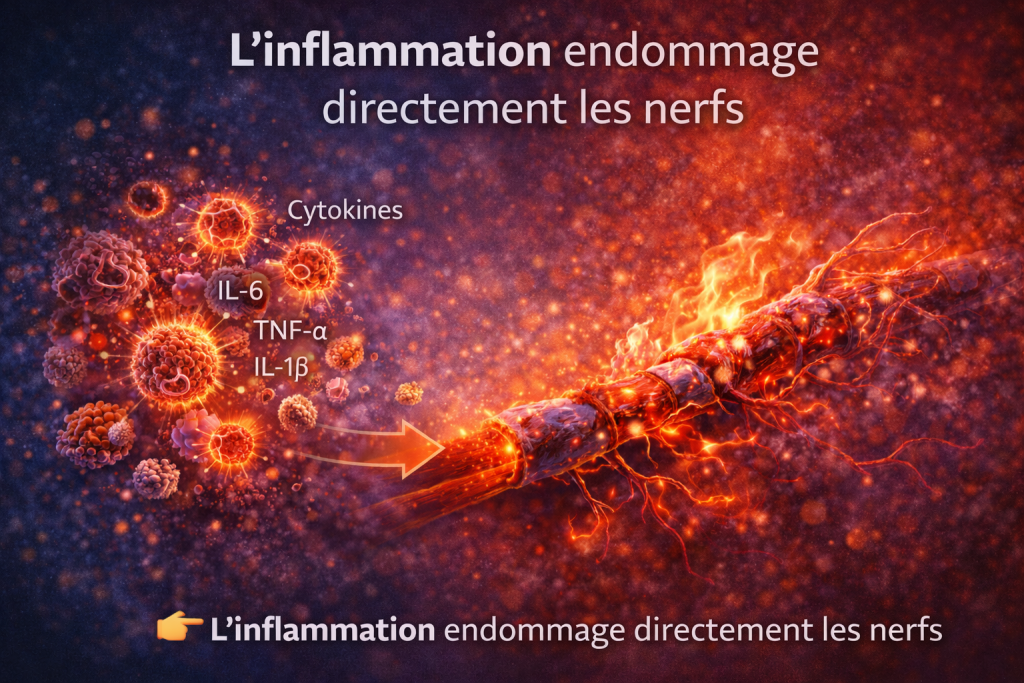
L’inflammation attaque les nerfs
Les cytokines pro-inflammatoires telles que l’IL-6, le TNF-α et l’IL-1β jouent un rôle clé dans la physiopathologie de la neuropathie.
Elles induisent :
- une altération de la conduction nerveuse
- une dégradation de la myéline
- une activation des nocicepteurs
Ces mécanismes contribuent à une hypersensibilité nerveuse et à la chronicisation de la douleur.
Des études ont montré que ces médiateurs inflammatoires sont significativement augmentés dans les neuropathies diabétiques et inflammatoires.
Références :
Vincent AM et al. Nat Rev Neurol. 2011.
Uçeyler N et al. Brain. 2009.
3.2 Neuroinflammation
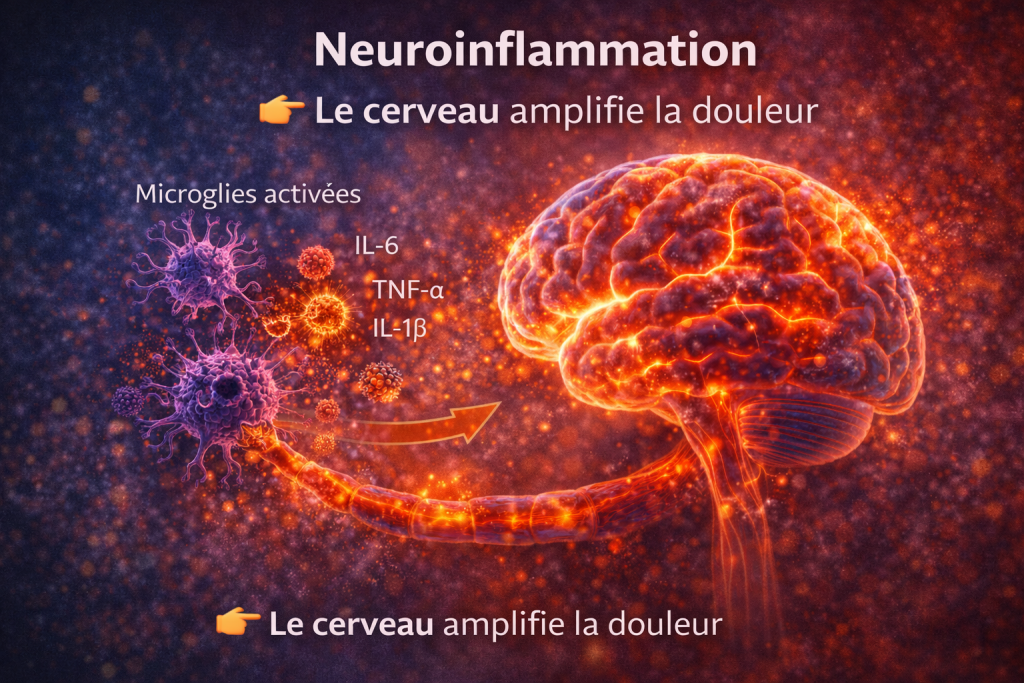
Le cerveau amplifie la douleur
La douleur neuropathique est amplifiée par des mécanismes centraux impliquant la neuroinflammation.
L’activation des cellules gliales, en particulier les microglies, entraîne la libération de médiateurs pro-inflammatoires au niveau du système nerveux central, amplifiant la transmission des signaux nociceptifs.
Ce phénomène de sensibilisation centrale explique la persistance de la douleur même en l’absence de lésion périphérique active.
Références :
Watkins LR et al. Trends Neurosci. 2001.
Ji RR et al. Nat Rev Neurosci. 2013.
Selon Linda Watkins :
« Les cellules gliales jouent un rôle central dans l’amplification des états douloureux.»
👉 Activation des microglies = amplification de la douleur chronique
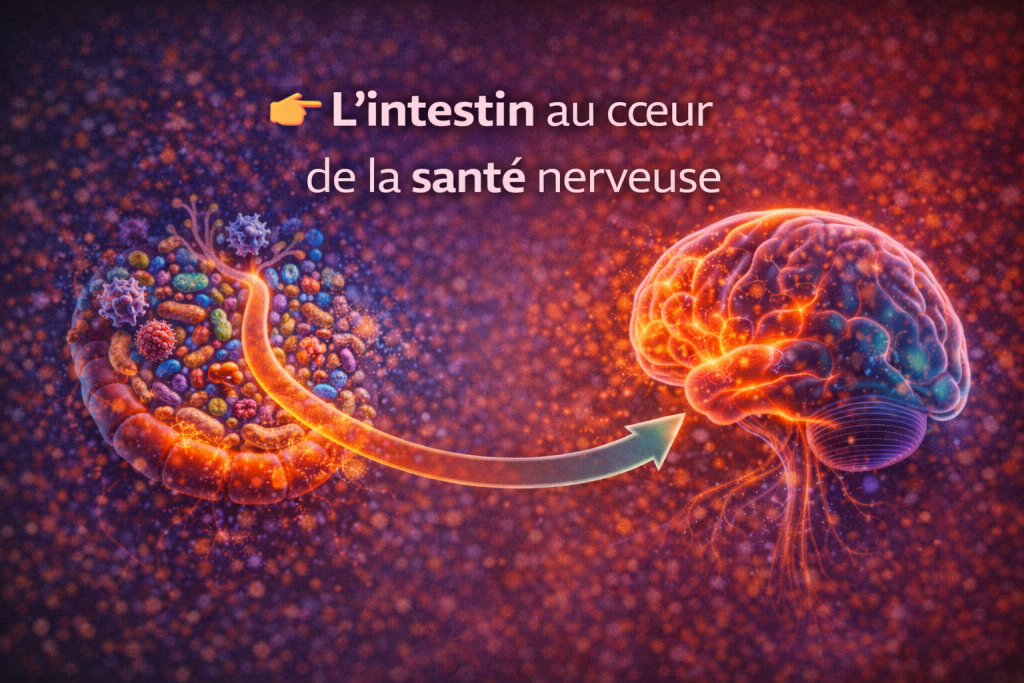
4. Microbiote intestinal et neuropathie
4.1 Axe intestin-cerveau
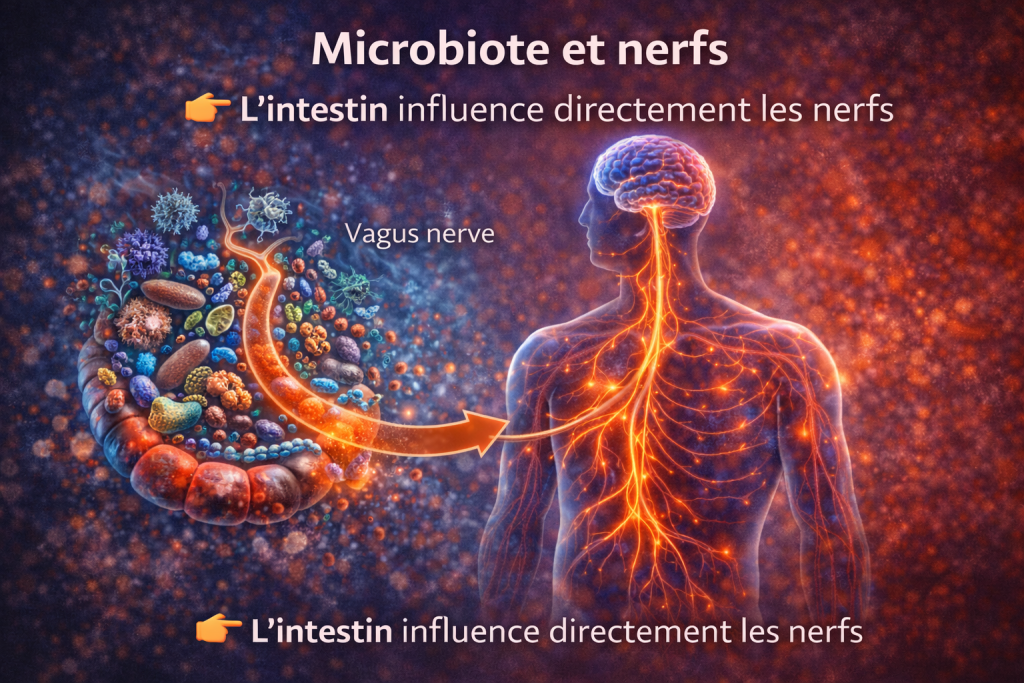
L’intestin pilote les nerfs
Le microbiote intestinal joue un rôle fondamental dans la régulation de l’immunité et de l’inflammation.
Il influence le système nerveux via l’axe intestin-cerveau, notamment par :
- la production de métabolites (SCFA)
- la modulation des cytokines
- l’interaction avec le nerf vague
Une dysbiose intestinale est associée à une augmentation de l’inflammation systémique et pourrait contribuer au développement de neuropathies.
Références :
Cryan JF et al. Physiol Rev. 2019.
Honda K, Littman DR. Nature. 2016.
Le microbiote influence :
- l’immunité
- l’inflammation
- la fonction nerveuse
4.2 Dysbiose et endotoxémie
Patrice D. Cani :
« Metabolic endotoxemia is a key trigger of systemic inflammation. »
👉 LPS → inflammation → atteinte nerveuse
5. Perméabilité intestinale et atteinte nerveuse
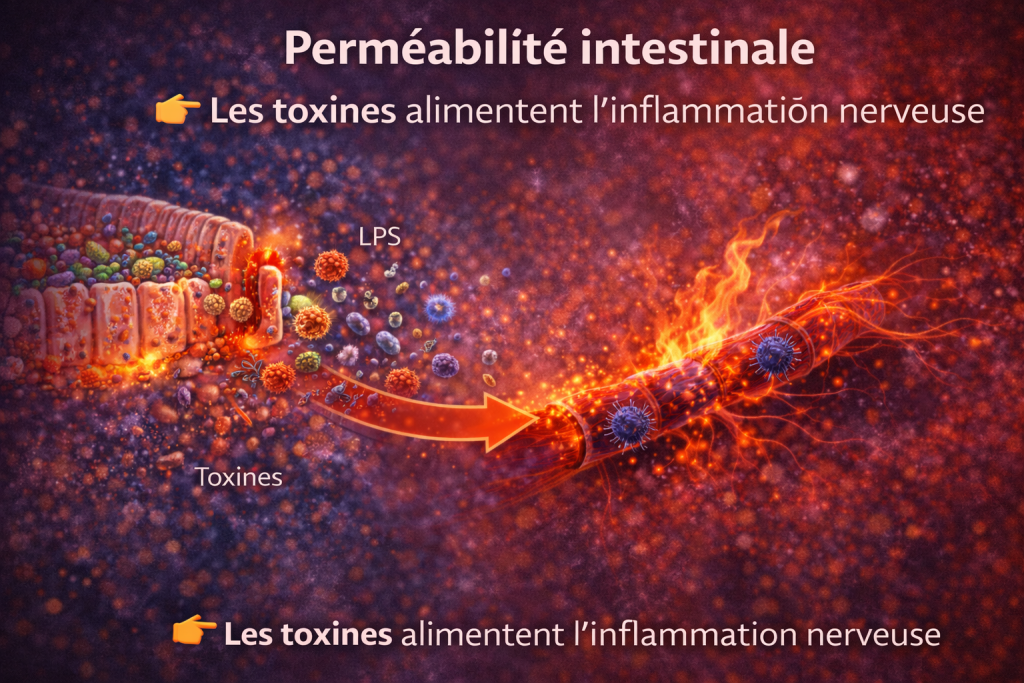
Une barrière intestinale altérée
La perméabilité intestinale accrue (“leaky gut”) permet le passage de lipopolysaccharides (LPS) dans la circulation sanguine.
Ces endotoxines bactériennes déclenchent une activation immunitaire systémique, contribuant à un état inflammatoire chronique.
Cette endotoxémie métabolique est impliquée dans de nombreuses pathologies, dont les troubles neurologiques et les neuropathies.
Références :
Cani PD et al. Diabetes. 2007.
Bischoff SC et al. Gut. 2014.
Une barrière intestinale altérée entraîne :
- passage de toxines
- activation immunitaire
- inflammation systémique
👉 impact direct sur les nerfs périphériques
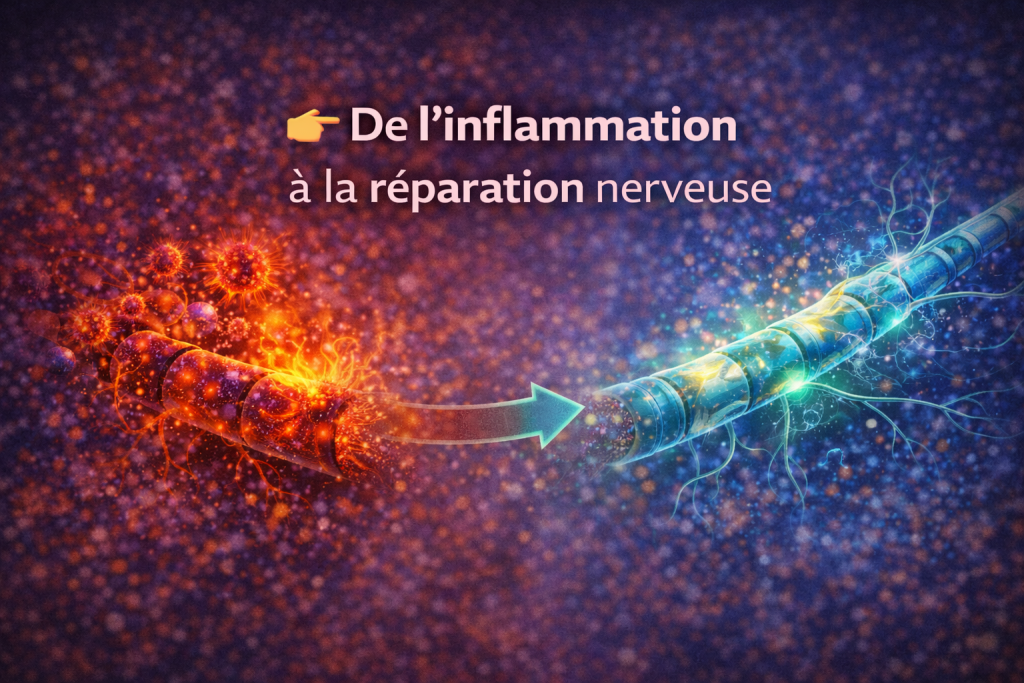
6. Neuropathie et stress oxydatif
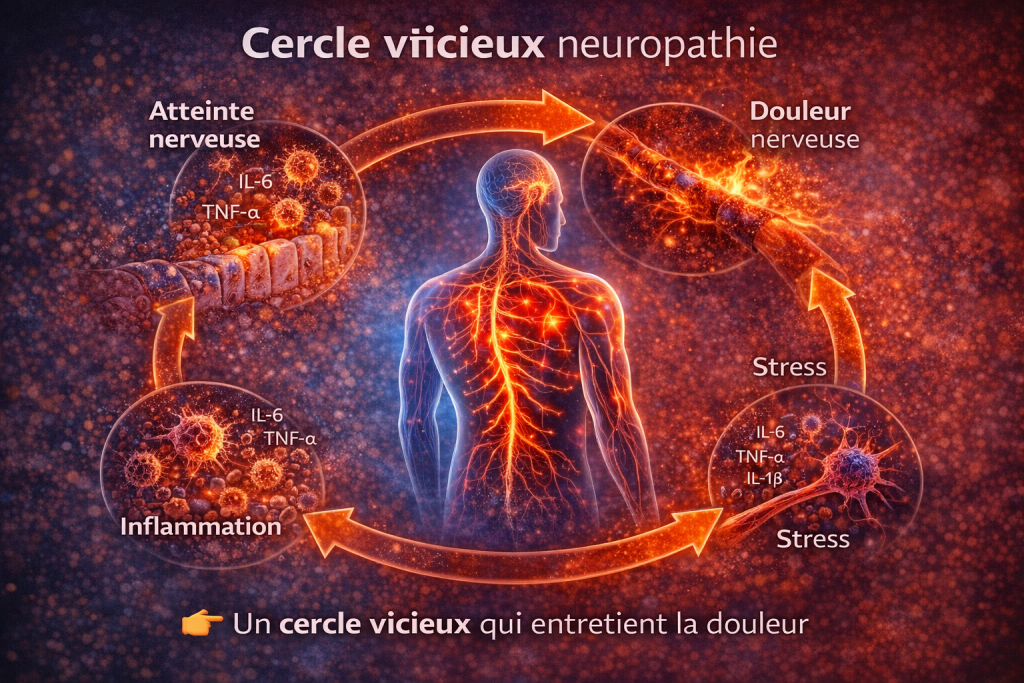
Le piège de la neuropathie
La neuropathie s’inscrit dans un cercle physiopathologique auto-entretenu :
- inflammation → douleur
- douleur → stress
- stress → inflammation
Ce cycle entraîne une amplification progressive des symptômes et une chronicisation de la pathologie.
La gestion de ce cercle vicieux constitue un enjeu thérapeutique majeur.
Références :
McEwen BS. Ann N Y Acad Sci. 2007.
Apkarian AV et al. Nat Rev Neurosci. 2009.
Le stress oxydatif :
- endommage les neurones
- altère les mitochondries
- aggrave la dégénérescence nerveuse
7. Causes fréquentes associées
- diabète
- syndrome métabolique
- carences (B1, B6, B12)
- alcool
- infections chroniques
- dysbiose intestinale
👉 point commun : inflammation chronique

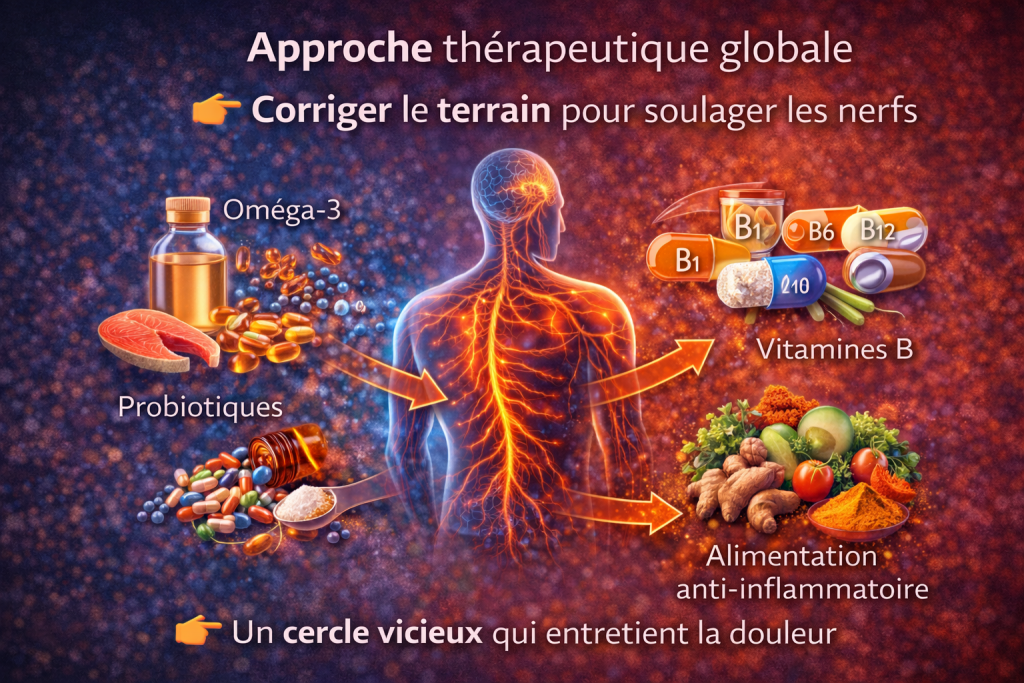
8. Approche thérapeutique intégrative
Corriger le terrain
Les approches thérapeutiques modernes s’orientent vers une vision intégrative visant à corriger les déséquilibres sous-jacents :
- réduction de l’inflammation
- modulation du microbiote
- soutien nutritionnel
Les acides gras oméga-3, notamment EPA et DHA, ont démontré des effets anti-inflammatoires significatifs en modulant la production de cytokines.
Références :
Calder PC. Nutrients. 2010.
Serhan CN. Nature. 2008.
8.1 Limites des traitements conventionnels
- antalgiques
- antiépileptiques
- antidépresseurs
👉 soulagent mais ne corrigent pas la cause

9. Protocole naturel structuré
⚠️ Approche complémentaire — ne remplace pas un suivi médical
Mesurer avant d’agir
L’évaluation biologique permet une prise en charge personnalisée.
Les marqueurs pertinents incluent :
- CRP ultrasensible
- profil en acides gras
- statut vitaminique
- analyse du microbiote
Ces données permettent d’identifier les déséquilibres et d’adapter les interventions thérapeutiques.
Références :
Calder PC et al. Br J Nutr. 2020.
Zhernakova A et al. Science. 2016.
Phase 1 : Évaluation
- CRP ultrasensible
- bilan oméga 3 / oméga 6
- vitamines B
- glycémie / insulinémie
- analyse du microbiote
Phase 2 : Réduction de l’inflammation
Objectifs :
- diminuer cytokines
- restaurer équilibre lipidique
Actions :
- augmenter oméga-3 (EPA/DHA)
- réduire sucres raffinés
- alimentation anti-inflammatoire
Selon Philip C. Calder :
«Les acides gras oméga-3 exercent de puissants effets anti-inflammatoires.»
Phase 3 : Rééquilibrage du microbiote
- fibres prébiotiques
- probiotiques ciblés
- polyphénols
👉 restaurer l’effet barrière
Phase 4 : Réparation intestinale
- glutamine
- zinc
- polyphénols
👉 réduire la perméabilité intestinale
Phase 5 : Soutien nerveux
- vitamines B (B1, B6, B12)
- acide alpha-lipoïque
- magnésium
👉 améliorer la conduction nerveuse
Phase 6 : Modulation du système nerveux
- gestion du stress
- sommeil
- activité physique modérée
10. Stratégie globale
Une approche sur-mesure
La variabilité interindividuelle des réponses biologiques impose une approche personnalisée.
La médecine de précision repose sur :
- l’analyse des biomarqueurs
- l’adaptation des interventions
- le suivi longitudinal
Cette approche améliore l’efficacité et la pertinence des stratégies thérapeutiques.
Références :
Ashley EA. JAMA. 2016.
Collins FS. N Engl J Med. 2015.
👉 Corriger le terrain permet :
- réduction de l’inflammation
- amélioration de la fonction nerveuse
- diminution des symptômes
11. Discussion
La neuropathie apparaît aujourd’hui comme une pathologie systémique, liée à :
- inflammation
- microbiote
- métabolisme
👉 approche réductionniste insuffisante
Téléchargez le protocole complet ici : Document PDF
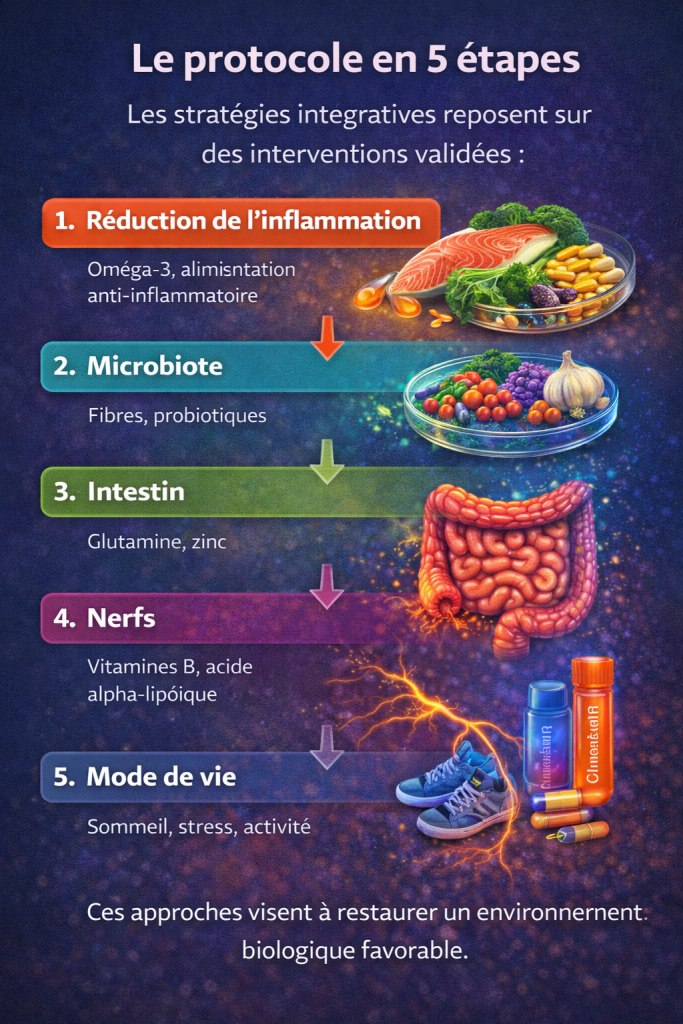
Le protocole en 5 étapes
Les stratégies intégratives reposent sur des interventions validées :
1. Réduction de l’inflammation
Oméga-3, alimentation anti-inflammatoire
2. Microbiote
Fibres, probiotiques
3. Intestin
Glutamine, zinc
4. Nerfs
Vitamines B, acide alpha-lipoïque
5. Mode de vie
Sommeil, stress, activité
Ces approches visent à restaurer un environnement biologique favorable.
Références :
Calder PC. Nutrients. 2010.
Vincent AM. Nat Rev Neurol. 2011.
Téléchargez le protocole complet ici : Document PDF
12. Conclusion
Restaurer le terrain
Les données scientifiques actuelles soutiennent une approche globale des neuropathies, intégrant inflammation, microbiote et métabolisme.
👉 La restauration du terrain biologique constitue une stratégie cohérente et prometteuse pour améliorer la qualité de vie des patients.
Références :
Furman D. Nat Med. 2019.
Les données scientifiques convergent vers une vision intégrative :
👉 la neuropathie n’est pas uniquement une maladie nerveuse
👉 c’est une manifestation d’un déséquilibre global
👉 restaurer le terrain = stratégie clé
L’évaluation du terrain biologique (inflammation, microbiote, statut nutritionnel) constitue aujourd’hui une étape essentielle dans la compréhension et la prise en charge des neuropathies.
Références
- Furman D et al. Chronic inflammation in the etiology of disease. Nat Med.
- Watkins LR et al. Glial activation in pain. Trends Neurosci.
- Cani PD et al. Metabolic endotoxemia. Diabetes.
- Calder PC. Omega-3 fatty acids and inflammation. Nutrients.
- Vincent AM et al. Oxidative stress in neuropathy. Nat Rev Neurol.
- Ziegler D. Diabetic neuropathy. Lancet.